
專(zhuān)注于審計(jì)追蹤、用戶(hù)管理以及數(shù)碼顯微鏡在生物技術(shù)和制藥行業(yè)細(xì)胞培養(yǎng)實(shí)驗(yàn)室中的優(yōu)勢(shì)

本文介紹了 FDA 21 CFR 第 11 部分的建議,特別關(guān)注細(xì)胞培養(yǎng)實(shí)驗(yàn)室中的審計(jì)追蹤和用戶(hù)管理。本文旨在為負(fù)責(zé)確保電子記錄和電子簽名符合 21 CFR 第 11 部分的生物技術(shù)和制藥行業(yè)專(zhuān)業(yè)人士提供指導(dǎo)。數(shù)碼顯微鏡方法,例如 Mateo FL,相較于紙質(zhì)方法,提供了更一致和高效的細(xì)胞培養(yǎng)結(jié)果電子文檔記錄的優(yōu)勢(shì)。
引言
細(xì)胞培養(yǎng)實(shí)驗(yàn)室越來(lái)越依賴(lài)電子系統(tǒng)進(jìn)行數(shù)據(jù)管理,因此遵守 FDA 法規(guī)至關(guān)重要。21 CFR(聯(lián)邦法規(guī))第 11 部分[1]概述了電子記錄和電子簽名被視為可信、可靠且等同于紙質(zhì)記錄的標(biāo)準(zhǔn)。本文將重點(diǎn)關(guān)注兩個(gè)關(guān)鍵方面:審計(jì)追蹤和用戶(hù)管理[1-3]。
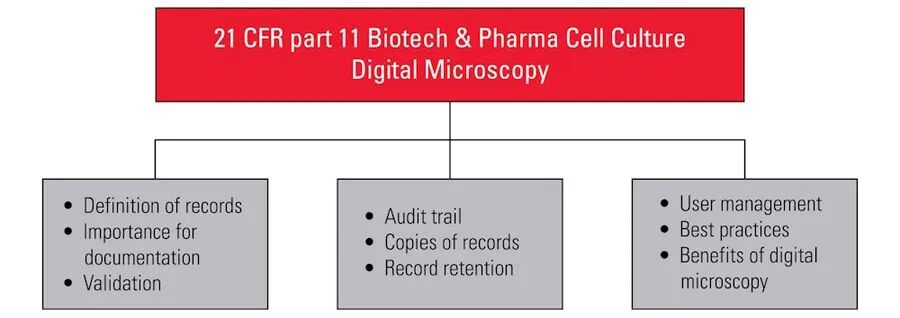
圖 1:示意圖概述了生物技術(shù)和制藥行業(yè)中關(guān)于細(xì)胞培養(yǎng)的電子記錄和簽名的 21 CFR 第 11 部分指南的基本步驟,以及數(shù)碼顯微鏡的使用。
21 CFR 第 11 部分概述
21 CFR 第 11 部分是由 FDA 引入的,旨在建立電子記錄和電子簽名的建議。該指南適用于制藥和生物技術(shù)行業(yè)中使用電子文檔的所有方面。涵蓋的關(guān)鍵領(lǐng)域包括系統(tǒng)驗(yàn)證、審計(jì)跟蹤、記錄保留和用戶(hù)訪問(wèn)控制。
范圍的解釋
為了促進(jìn)創(chuàng)新和技術(shù)進(jìn)步以造福公共健康,并避免不必要的控制和成本,F(xiàn)DA 打算狹義地解釋第 11 部分的范圍[1]。這意味著,對(duì)于需要維護(hù)或提交給 FDA 的記錄,當(dāng)這些記錄以電子格式而非紙質(zhì)格式使用時(shí),第 11 部分將適用。然而,這一事實(shí)不適用于電子記錄的紙質(zhì)打印件,當(dāng)紙質(zhì)記錄已用于滿(mǎn)足所有適用的 FDA 法規(guī)和規(guī)定的要求時(shí)。
第 11 部分記錄的定義
第 11 部分適用于以下電子記錄[1]:
以電子格式維護(hù)的記錄,可以替代或補(bǔ)充紙質(zhì)格式。
以電子格式提交給 FDA 的記錄。
用于執(zhí)行受監(jiān)管活動(dòng)的電子記錄,除了紙質(zhì)文件外。
替代手寫(xiě)簽名和其他簽署方式的電子簽名。
注意:建議需要維護(hù)的記錄的用戶(hù)提前確定受監(jiān)管活動(dòng)將如何執(zhí)行,即以電子形式還是紙質(zhì)形式。此決定應(yīng)明確記錄。
細(xì)胞培養(yǎng)結(jié)果文檔的重要性
遵循 21 CFR 第 11 部分的建議對(duì)于生物技術(shù)和制藥行業(yè)的細(xì)胞培養(yǎng)實(shí)驗(yàn)室至關(guān)重要,以確保數(shù)據(jù)完整性、可追溯性和問(wèn)責(zé)制。不遵循這些建議可能會(huì)導(dǎo)致重大處罰,包括產(chǎn)品召回、法律后果和市場(chǎng)信任的喪失。
驗(yàn)證
驗(yàn)證計(jì)算機(jī)系統(tǒng)的決定應(yīng)考慮用戶(hù)是否能夠滿(mǎn)足要求,并確保記錄和簽名的準(zhǔn)確性、真實(shí)性和完整性[1]。FDA 建議該方法應(yīng)基于文檔化的風(fēng)險(xiǎn)評(píng)估,以確定系統(tǒng)可能如何影響產(chǎn)品質(zhì)量、安全性和記錄完整性。
審計(jì)跟蹤建議
定義
審計(jì)跟蹤是一個(gè)安全的、計(jì)算機(jī)生成的、帶時(shí)間戳的電子記錄,允許重建與電子記錄的創(chuàng)建、修改或刪除相關(guān)的事件。
監(jiān)管建議
根據(jù) 21 CFR 第 11 部分,審計(jì)跟蹤應(yīng):
記錄操作員輸入和操作的日期和時(shí)間;
具有安全性并防止未經(jīng)授權(quán)的訪問(wèn);
以便于檢索和審查的方式存儲(chǔ);
捕捉對(duì)關(guān)鍵數(shù)據(jù)的更改,例如細(xì)胞培養(yǎng)條件和結(jié)果。
實(shí)施
為了實(shí)施有效的審計(jì)追蹤:
使用自動(dòng)記錄所有用戶(hù)操作的軟件;
確保所有修改都有時(shí)間戳條目;
定期審查和審核記錄軌跡,以查找不一致或未經(jīng)授權(quán)的更改。
應(yīng)遵守所有關(guān)于文檔的要求,例如日期和時(shí)間[1]。如果沒(méi)有這樣的要求,審計(jì)軌跡或其他物理、邏輯或程序安全措施仍然可能對(duì)確保記錄的可信性和可靠性至關(guān)重要。決策應(yīng)基于定義的要求、風(fēng)險(xiǎn)評(píng)估、記錄完整性以及產(chǎn)品質(zhì)量/安全性。
此外,當(dāng)受監(jiān)管記錄的創(chuàng)建、修改或刪除發(fā)生時(shí),審計(jì)軌跡可能會(huì)很有用。
記錄的副本
在檢查期間,應(yīng)向調(diào)查人員提供適當(dāng)?shù)挠涗浽L問(wèn)權(quán)限[1]。電子記錄的副本應(yīng)以常見(jiàn)的電子格式(PDF、XML 或 SGML)提供,使用已建立的軟件轉(zhuǎn)換或?qū)С龇椒āK褂玫膹?fù)制過(guò)程應(yīng)生成保留記錄內(nèi)容和含義的副本。應(yīng)允許在組織的場(chǎng)所使用其硬件對(duì)記錄進(jìn)行可讀形式的檢查、審查和復(fù)制。
記錄保留
維護(hù)記錄的決策應(yīng)基于定義的要求和記錄的風(fēng)險(xiǎn)評(píng)估,包括對(duì)記錄隨時(shí)間變化的價(jià)值的判斷[1]。重要的是,任何所需記錄的副本應(yīng)保留其內(nèi)容和含義。記錄可以以非電子格式歸檔,例如微縮膠卷、微縮膠片和紙張,或以標(biāo)準(zhǔn)電子文件格式(例如 PDF、XML 或 SGML)歸檔。此外,電子和非電子記錄及簽名可以共存,即混合情況。
用戶(hù)管理建議
定義
用戶(hù)管理涉及控制和監(jiān)控對(duì)電子系統(tǒng)的訪問(wèn),以確保只有授權(quán)個(gè)人可以執(zhí)行特定任務(wù)。
監(jiān)管要求
21 CFR 第 11 部分的要求:
所有訪問(wèn)系統(tǒng)的個(gè)人必須使用唯一的用戶(hù) ID 和密碼;
根據(jù)工作職責(zé)分配角色和權(quán)限;
定期審查和更新用戶(hù)訪問(wèn)權(quán)限;
立即撤銷(xiāo)已終止或調(diào)動(dòng)員工的訪問(wèn)權(quán)限。
實(shí)施
可以通過(guò)有效的用戶(hù)管理來(lái)實(shí)現(xiàn):
實(shí)施基于角色的訪問(wèn)控制(RBAC);
定期進(jìn)行安全協(xié)議培訓(xùn)課程;
定期審計(jì)用戶(hù)訪問(wèn)日志;
使用多因素身份驗(yàn)證(MFA)以增強(qiáng)安全性。
合規(guī)的最佳實(shí)踐
系統(tǒng)驗(yàn)證
驗(yàn)證所有電子系統(tǒng)以確保其符合 21 CFR 第 11 部分的要求,包括驗(yàn)證審計(jì)跟蹤和用戶(hù)管理功能是否正常運(yùn)行。
文檔
維護(hù)所有合規(guī)活動(dòng)的全面文檔,包括用戶(hù)訪問(wèn)審查、系統(tǒng)驗(yàn)證和審計(jì)跟蹤審計(jì)。
定期審計(jì)
定期進(jìn)行內(nèi)部審計(jì),以識(shí)別和糾正任何合規(guī)差距。邀請(qǐng)第三方審計(jì)員進(jìn)行公正評(píng)估。
培訓(xùn)
為所有人員提供關(guān)于 21 CFR 第 11 部分合規(guī)性的重要性持續(xù)培訓(xùn),重點(diǎn)關(guān)注審計(jì)追蹤和用戶(hù)管理。
Mateo FL 數(shù)碼顯微鏡的優(yōu)勢(shì)
為幫助用戶(hù)遵循 21 CFR 第 11 部分的建議,Mateo FL 顯微鏡提供以下功能:
關(guān)于驗(yàn)證、審計(jì)追蹤和用戶(hù)管理(上述第 4、5 和 8 節(jié))
內(nèi)置詳細(xì)的審計(jì)追蹤和集成的用戶(hù)管理功能,以便于更輕松和更安全的數(shù)據(jù)管理;
通過(guò)條形碼掃描功能輕松跟蹤和管理樣本。
關(guān)于記錄的副本和記錄保留(上述第 6 和第 7 節(jié))
通過(guò)二維碼更輕松地將數(shù)據(jù)共享到任何移動(dòng)設(shè)備;
安全的數(shù)據(jù)跟蹤和無(wú)縫的數(shù)據(jù)傳輸;
更實(shí)用的文件存儲(chǔ)管理 - 可存儲(chǔ)高達(dá) 300 萬(wàn)張圖片,擁有 500GB 的存儲(chǔ)空間,從而減少傳輸或刪除文件的時(shí)間。
Mateo FL 如何幫助用戶(hù)滿(mǎn)足 21 CFR 第 11 部分關(guān)于驗(yàn)證、審計(jì)跟蹤、記錄副本、記錄保留和用戶(hù)管理的建議的示例如下圖 2 和圖 3 所示。
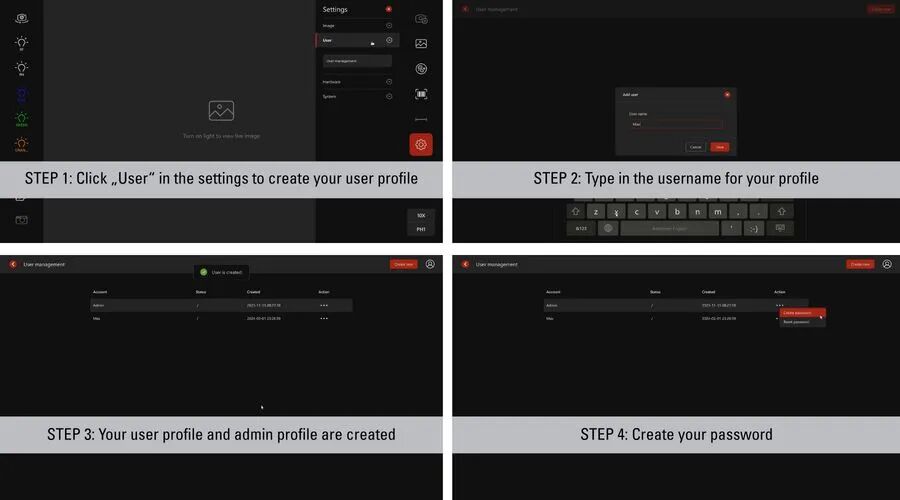
圖2:只需4次點(diǎn)擊即可創(chuàng)建用戶(hù)個(gè)人資料。
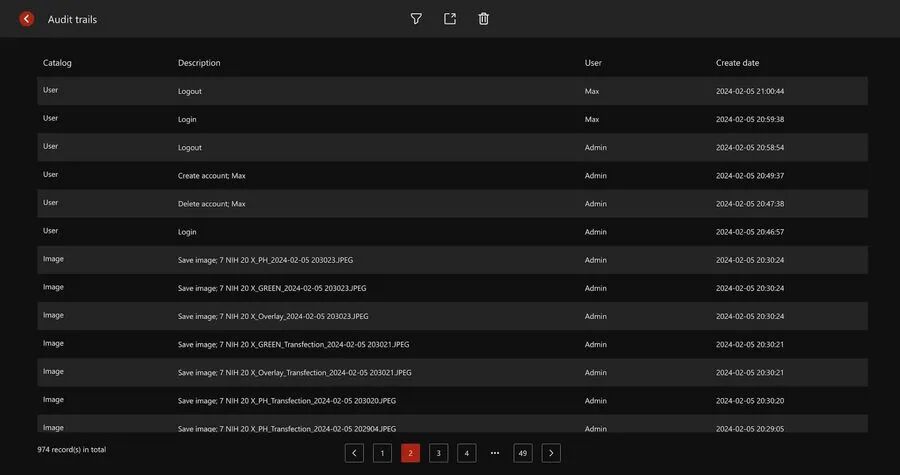
圖 3:用戶(hù)活動(dòng)的記錄保持。
結(jié)論
遵守 21 CFR 第 11 部分對(duì)于確保生物技術(shù)和制藥細(xì)胞培養(yǎng)實(shí)驗(yàn)室電子記錄的完整性和可靠性至關(guān)重要。通過(guò)專(zhuān)注于強(qiáng)大的審計(jì)跟蹤和用戶(hù)管理實(shí)踐,組織可以滿(mǎn)足監(jiān)管要求并保持最高的數(shù)據(jù)安全性和可追溯性標(biāo)準(zhǔn)。與基于紙張的記錄相比,使用數(shù)碼顯微鏡方法進(jìn)行細(xì)胞培養(yǎng)在電子記錄方面的優(yōu)勢(shì)在于結(jié)果的記錄更加一致和高效。

常見(jiàn)問(wèn)題解答

什么是 21 CFR 第 11 部分,為什么它很重要?
21 CFR 第 11 部分是美國(guó)食品藥品監(jiān)督管理局(FDA)針對(duì)電子記錄和電子簽名的指導(dǎo)方針。它幫助用戶(hù)確保電子記錄與紙質(zhì)記錄同樣可靠,這對(duì)于在生物技術(shù)和制藥等受監(jiān)管環(huán)境中維護(hù)數(shù)據(jù)完整性和可追溯性至關(guān)重要。
Mateo FL 顯微鏡如何幫助滿(mǎn)足 21 CFR 第 11 部分的合規(guī)要求?
Mateo FL 提供了合規(guī)所需的審計(jì)追蹤和用戶(hù)管理功能。它自動(dòng)記錄所有用戶(hù)操作,并跟蹤對(duì)記錄所做的任何修改,確保數(shù)據(jù)管理的安全性和可追溯性。
Mateo FL 的哪些功能有助于安全的數(shù)據(jù)管理?
Mateo FL 允許詳細(xì)的審計(jì)追蹤。此外,它通過(guò)二維碼提供無(wú)縫的數(shù)據(jù)傳輸,并支持長(zhǎng)期數(shù)據(jù)存儲(chǔ),這對(duì)于合規(guī)性至關(guān)重要。
Mateo FL 顯微鏡的審計(jì)追蹤功能可以自定義嗎?
Mateo FL 的審計(jì)追蹤是內(nèi)置的,捕捉所有相關(guān)操作。管理員可以審查審計(jì)追蹤,以驗(yàn)證操作是否符合監(jiān)管標(biāo)準(zhǔn)。當(dāng)啟用時(shí),它會(huì)記錄并保護(hù)所有數(shù)據(jù),以實(shí)現(xiàn)全面可追溯性,支持符合 21 CFR 第 11 部分的要求。
Mateo FL 如何處理數(shù)據(jù)存儲(chǔ)和保留以確保合規(guī)?
Mateo FL 提供了 500 GB 的寬裕存儲(chǔ)空間,能夠存儲(chǔ)多達(dá) 300 萬(wàn)張圖像,確保數(shù)據(jù)安全保留,無(wú)需頻繁轉(zhuǎn)移,從而降低合規(guī)風(fēng)險(xiǎn)。
不遵循 21 CFR 第 11 部分建議的后果是什么?
不遵循 21 CFR 第 11 部分的建議可能導(dǎo)致不符合 FDA 對(duì)生物技術(shù)和制藥行業(yè)的規(guī)定,可能會(huì)導(dǎo)致重大處罰,包括罰款、產(chǎn)品召回、法律訴訟和市場(chǎng)信任的喪失。實(shí)施 Mateo FL 有助于您的實(shí)驗(yàn)室滿(mǎn)足監(jiān)管要求。
免責(zé)聲明:
本文件中提供的 21 CFR 第 11 部分概述并不構(gòu)成法律建議或任何其他具有約束力的建議。此概述中包含的所有信息僅供一般信息參考。閱讀此概述的讀者應(yīng)聯(lián)系其顧問(wèn)或律師,以獲取有關(guān)任何特定事項(xiàng)的建議。只有個(gè)別顧問(wèn)或律師才能保證此概述中包含的信息適用于特定情況或適合特定情況。沒(méi)有任何聲明表明該概述的內(nèi)容是完整或無(wú)誤的。
參考文獻(xiàn):
1.CFR - 聯(lián)邦法規(guī)第 21 卷,第 11 部分,電子記錄;電子簽名 - 范圍和適用性,行業(yè)指南,2003 年,美國(guó)食品和藥物管理局(FDA)。
2.ISPE 指導(dǎo)文件,GAMP® 5:基于風(fēng)險(xiǎn)的合規(guī) GxP 計(jì)算機(jī)系統(tǒng)方法,第 2 版,國(guó)際制藥工程學(xué)會(huì) (ISPE)。
3.PDA 技術(shù)報(bào)告第 80 號(hào) (TR 80):制藥實(shí)驗(yàn)室的數(shù)據(jù)完整性管理系統(tǒng)(單用戶(hù)數(shù)字版),注射藥物協(xié)會(huì) (PDA)。
相關(guān)產(chǎn)品
Mateo FL數(shù)字顯微鏡

電話(huà)
微信掃一掃
